ICLUSIG falsifié commercialisé au niveau mondial
Falsified ICLUSIG traded globally
Cette alerte concerne des versions falsifiées confirmées d'ICLUSIG 15 mg et d'ICLUSIG 45 mg en circulation dans les régions OMS de l’Europe et des Amériques. Genuine ICLUSIG, La forme authentique d’ICLUSIG, dont l’ingrédient pharmaceutique actif est le Ponatinib Hydrochloride, permet de traiter différentes formes de leucémie.
Le 15 janvier 2019, les autorités sanitaires Suisses ont informé l'OMS qu’un grossiste local avait acheté des p boites d'ICLUSIG 15 mg : après vérification, le titulaire de l'autorisation de mise sur le marché a confirmé la falsification. Une enquête plus approfondie a établi que deux versions falsifiées d'ICLUSIG étaient commercialisées au niveau mondial, y compris au travers de ventes par Internet. Ces produits sont détaillés dans le tableau ci-dessous :
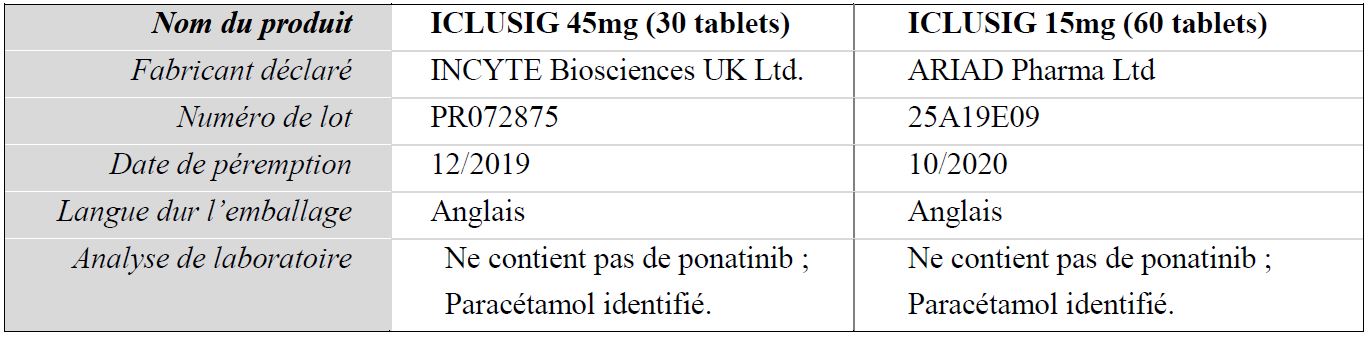
L’analyse en laboratoire d’ICLUSIG 15 mg, numéro de lot 25A19E09, a confirmé que le produit ne contient pas de Ponatinib, mais contient à la place du paracétamol.
L’analyse en laboratoire d’ICLUSIG 45 mg, numéro de lot PR072875, a confirmé que le produit ne contient pas de Ponatinib, mais contient à la place du paracétamol.
ICLUSIG est commercialisé par différentes parties prenantes dans différentes parties du monde. Les sociétés pharmaceutiques TAKEDA et INCYTE sont les véritables fabricants et détenteurs de l’autorisation de mise sur le marché d’ICLUSIG dans les régions où les versions falsifiées susmentionnées ont été découvertes à ce jour, ces deux entreprises ont confirmé à l’OMS:
- qu’elles n’avaient pas fabriqué ni fourni les produits ci-dessus, et
- que les numéros de lot ci-dessus ne correspondent pas aux archives de fabrication authentiques.
Les photographies disponibles sont en dessous.
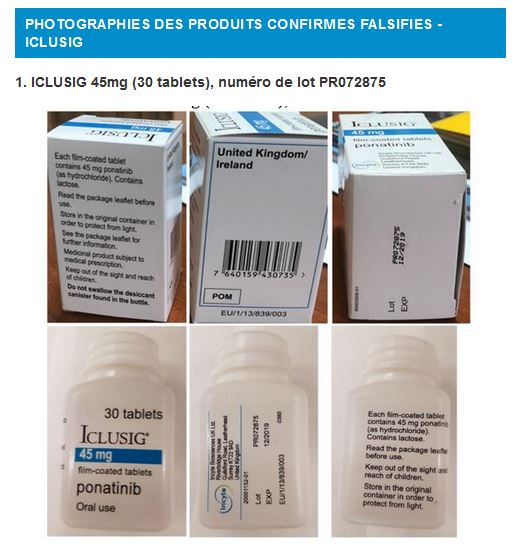
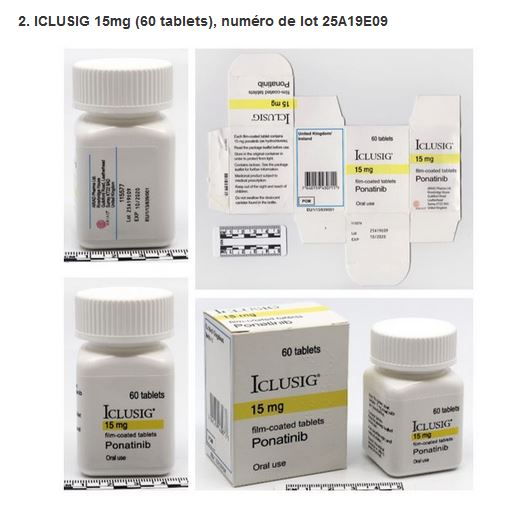
L’OMS recommande une vigilance accrue au sein des chaînes d’approvisionnement dans les pays susceptibles d’être concernés par ces produits falsifiés. Ce besoin de vigilance accrue s’applique également aux hôpitaux, dispensaires, centres de santé, grossistes, distributeurs, pharmacies et tout autre fournisseur de produits médicaux.
Si vous êtes en possession de ce produit, veuillez ne pas l’utiliser. Si toutefois vous avez pris ce produit falsifié ou si vous souffrez d’effets indésirables, un manque d’efficacité thérapeutique inattendu, suite à sa consommation, veuillez immédiatement consulter un professionnel de la santé qualifié et signaler cet incident à votre ministère de la santé, autorité nationale de réglementation du médicament ou centre national de pharmacovigilance.
Tout produit médical doit être obtenu auprès de sources authentiques et fiables. L’authenticité et l’état du produit doivent être soigneusement vérifiés. En cas de doute, demandez conseil à un professionnel de la santé.
Les autorités sanitaires nationales sont priées d’informer immédiatement l’OMS si ce type de produit falsifié est découvert dans leur pays. Si vous avez des informations concernant la fabrication, la distribution ou la circulation de ces produits, veuillez contacter rapidalert@who.int
Système Mondial de Surveillance et de Suivi des produits médicaux de qualité inférieure et falsifiésPour plus d’informations, visitez notre site Web : http://covid.comesa.int/medicines/publications/drugalerts/en/
Pour recevoir les alertes de l’OMS sur les produits médicaux : http://covid.comesa.int/about/licensing/rss/en/
