ICLUSIG falsifié disponible au niveau des patients en Asie et commercialisé au niveau mondial
ICLUSIG falsifié disponible au niveau des patients en Asie et commercialisé au niveau mondial
Cette alerte produit médical concerne des versions confirmées falsifiées d’ICLUSIG 45 mg en circulation dans la Région OMS du Pacifique occidental ; elle est liée à Alerte produit médical N° 2/2019 publiée le 31 janvier 2019 concernant des produits ICLUSIG falsifiés commercialisés au niveau mondial. La forme authentique d’ICLUSIG, dont le principe actif est le ponatinib (sous forme de chlorhydrate), est utilisée pour traiter différentes formes de leucémie.
Le 18 février 2019, l’OMS a été informée qu’un grossiste basé en Malaisie avait acheté le produit ICLUSIG 45 mg portant le numéro de lot PR072875, présenté dans un emballage en langue anglaise. Ce produit est déjà référencé dans la précédente Alerte produit médical N° 2/2019 et est confirmé falsifié.
Le même grossiste avait également acheté ICLUSIG 45 mg portant le numéro de lot PR0834170, présenté dans un emballage en langue allemande. Après vérification, le fabricant mentionné sur l’emballage a confirmé que ce produit est également falsifié.
Les informations relatives aux deux produits falsifiés détectés en Malaisie sont résumées dans le tableau ci dessous.
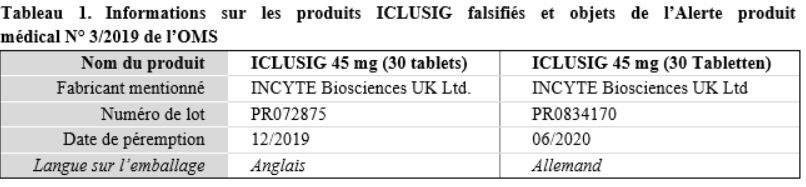
À ce stade, aucune analyse en laboratoire n’a encore été effectuée sur les échantillons provenant de Malaisie. Les deux produits étaient disponibles au niveau des patients.
Des échantillons issus des deux produits ICLUSIG falsifiés référencés dans la précédente Alerte produit médical N° 2/2019 de l’OMS ont été analysés (ICLUSIG 45 mg portant le numéro de lot PR072875 et ICLUSIG 15 mg portant le numéro de lot 25A19E09). Les résultats de laboratoire montrent que, dans les deux cas, le principe actif attendu, le ponatinib, est absent et remplacé par du paracétamol.
ICLUSIG est commercialisé par différentes parties prenantes dans différentes parties du monde. Les laboratoires pharmaceutiques TAKEDA et INCYTE sont les véritables fabricants d’ICLUSIG et ils ont tous deux confirmé à l’OMS :
- qu’ils ne fabriquaient pas et ne fournissaient pas les produits susmentionnés ;
- que le numéro de lot PR0834170 ne correspond pas aux registres de fabrication authentiques ;
- que le numéro de lot PR072875 combiné à l’emballage en langue anglaise ne correspond pas aux registres de fabrication authentiques.
Les photos sont disponibles ci-dessous
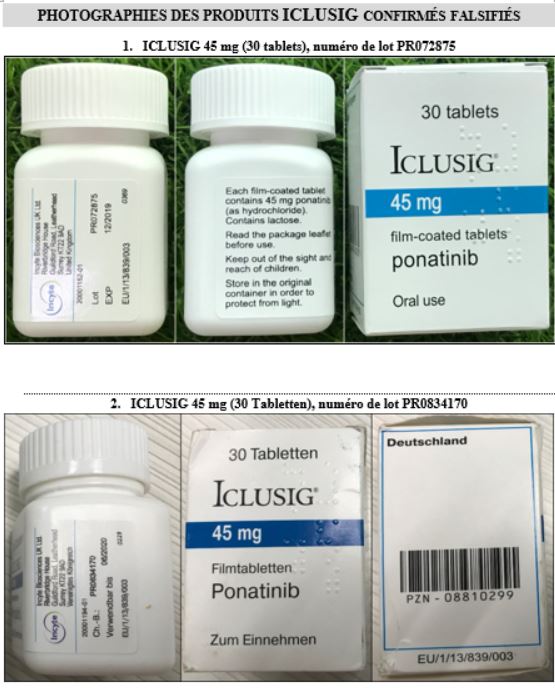
L’OMS recommande une vigilance accrue au niveau des chaînes d’approvisionnement dans les pays susceptibles d’être concernés par ces produits falsifiés. Cette vigilance renforcée s’applique aux hôpitaux, dispensaires, centres de santé, grossistes, distributeurs, pharmacies et tout autre fournisseur de produits médicaux.
Si vous êtes en possession de ces produits, veuillez ne pas les utiliser. Si toutefois vous avez pris un de ces produits falsifiés ou si vous souffrez de manifestations indésirables ou d’un manque d’efficacité inattendu, veuillez consulter immédiatement un professionnel de la santé qualifié et vous assurer qu’il notifie cet incident au Ministère de la santé, à l’Autorité nationale de réglementation du médicament ou au Centre national de pharmacovigilance.
Tout produit médical doit être obtenu auprès de sources authentiques et fiables. L’authenticité et l’état du produit doivent être soigneusement vérifiés. En cas de doute, demandez conseil à un professionnel de la santé.
Les autorités sanitaires nationales sont priées d’informer immédiatement l’OMS si ces produits falsifiés sont découverts dans leur pays. Si vous avez des informations concernant la fabrication, la distribution ou la circulation de ces produits, veuillez écrire à rapidalert@who.int
Système mondial OMS de surveillance et de suivi des produits médicaux de qualité inférieure et falsifiésPour plus d’informations, visitez notre site Web :http://covid.comesa.int/medicines/publications/drugalerts/en/
To sign up for WHO Medical Product Alerts, please visit: http://covid.comesa.int/about/licensing/rss/en/
